경제
셀트리온, 대웅제약 3차 임상 지원대상 선정, 2월 초 허가 전망
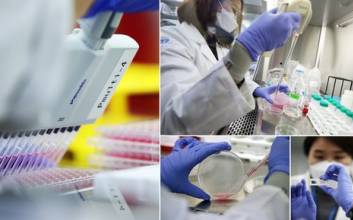
정부가 코로나19 치료제와 백신 개발에 대한 임상지원을 확대한다. 권덕철 보건복지부 장관은 26일 '코로나19 치료제·백신 임상지원 3차 공모'를 진행한 결과 셀트리온, 대웅제약이 각각 개발 중인 치료제 2종과 셀리드, 유바이오로직스가 각각 연구 중인 백신 2종을 임상지원 대상으로 선정했다고 발표했다. 이로써 복지부가 임상지원 중인 코로나19 치료제·백신은 총 10종(치료제 5·백신 5)으로 늘어났다. 현재까지 복지부가 치료제·백신 10종 개발 지원에 들인 예산은 약 1208억원이다. 복지부는 코로나19 치료제와 백신 개발을 지원하기 위해 국가신약개발사업단을 통해 격월로 임상지원 과제를 공모하고 있다. 치료제와 백신 개발을 지원하기 위한 예산도 지난해 940억원에서 올해 1388억원으로 48% 늘어났다. 복지부는 지난해 9월부터 '국가감염병임상시험센터'를 통해 피시험자를 모집해 치료제·백신이 신속하게 개발될 수 있도록 지원해왔다. 또 민간기업들이 연구를 진행하면서 겪는 애로사항을 해결하기 위해 상담창구인 '임상시험지원 TF(태스크포스)'를 운영하고, '기업애로사항해소지원센터'를 설치해 문제 해결도 지원하고 있다. 한편 식품의약품안전처는 코로나 치료제를 2월 초, 백신을 2월 둘째 주에 허가한다는 계획이다. 셀트리온 치료제가 가장 먼저 허가를 받을 것으로 보인다. 백신은 아스트라제네카와 화이자 백신이 앞선 상황이다. 정부당국은 올해 백신 5건, 치료제 3건 도입을 목표로 하고 있다. 치료제는 셀트리온의 항체치료제를 비롯해 대웅제약과 종근당, GC녹십자가 개발 중인 치료제가 주목 받고 있다. 김두용 기자 kim.duyong@joongang.co.kr
2021.01.26 12:16
















![세입자 낀 매물 ‘퇴로’ 열린다…정부, 양도세 중과 유예 종료 보완[only 이데일리]](https://image.edaily.co.kr/images/Photo/files/NP/S/2026/02/PS26020300714T.jpg)


![[포토]채수빈, 호기심 발동!](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000212.400x280.0.jpg)
![[포토]채수빈, 작은 얼굴에 '도대체 몇등신이야?"](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000211.400x280.0.jpg)
![[포토]채수빈, 미소로 주위를 밝히는 마법 시전](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000207.400x280.0.jpg)
![[포토]채수빈, 수줍은 미소](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000206.400x280.0.jpg)
![[포토]채수빈, 눈빛만으로 '분위기 여신'](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000204.400x280.0.jpg)
![[포토]채수빈, 현실감 떨어지는 비율](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000203.400x280.0.jpg)
![[포토]채수빈, 청순함 가득 담아 '하트'](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000202.400x280.0.jpg)
![[포토]채수빈, 오늘은 하트 요정](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000201.400x280.0.jpg)
![[포토]채수빈, 하트 더하기 애교](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000200.400x280.0.jpg)
![[포토]채수빈, 팬들 선물에 함박미소](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000199.400x280.0.jpg)
![[포토]채수빈, 청순 하트](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000198.400x280.0.jpg)
![[포토]이주빈, 날씨만큼 화사한 출국길](https://image.isplus.com/data/isp/image/2026/02/01/isp20260201000182.400x280.0.jpg)
